
Green Chemistry p. 4040 - 4045 (2019)
Update date:2022-08-11
Topics:
 Liu, Shujuan
Liu, Shujuan
 Dai, Xingchao
Dai, Xingchao
 Wang, Hongli
Wang, Hongli
 Shi, Feng
Shi, Feng
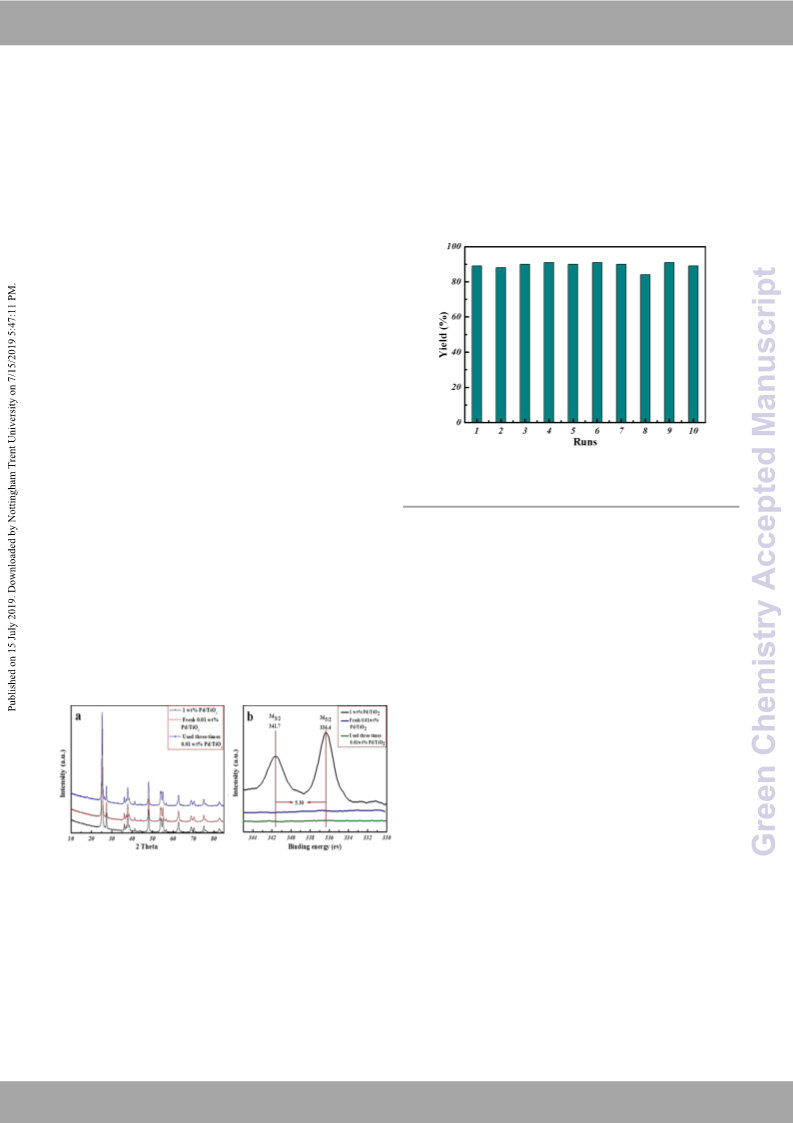
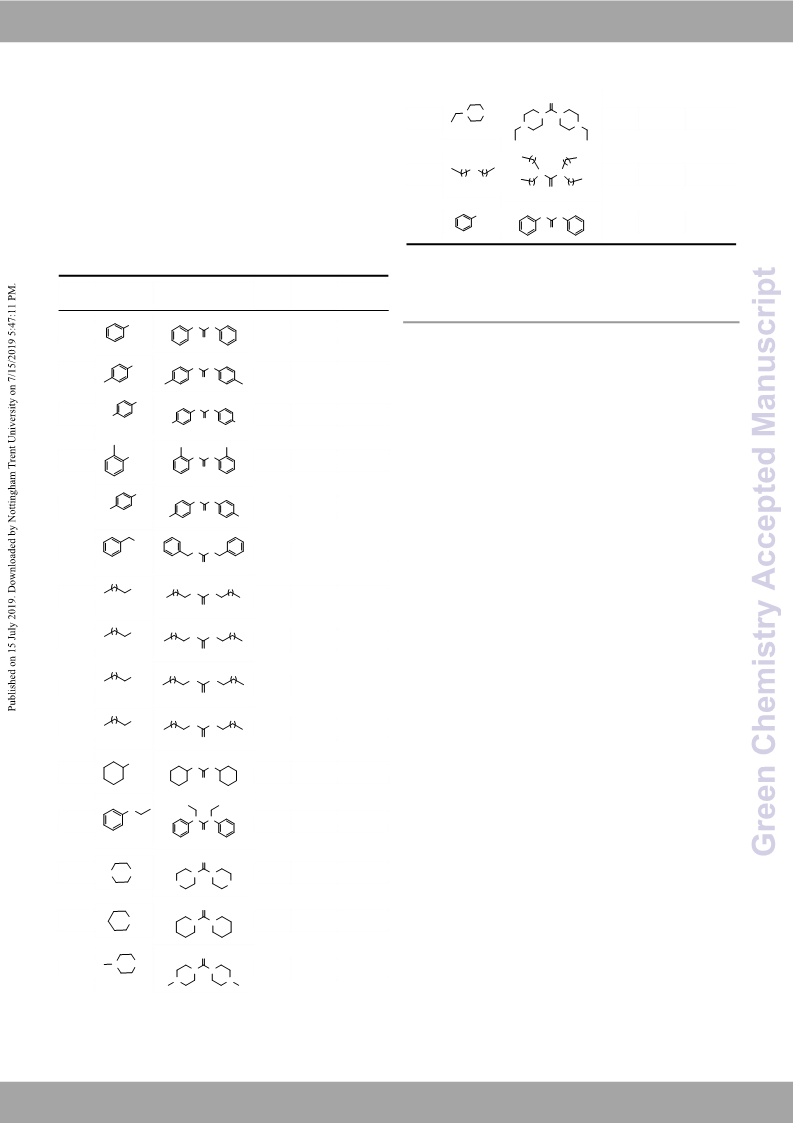
A highly active Pd/TiO2 catalyst system was prepared and applied in the oxidative carbonylation of amines to ureas with ultra-low Pd content under organic ligand and solvent free conditions. The catalytic turnover frequencies (TOFs, moles of amines converted per mole of Pd per h) were 126000 and 250000 h-1 for the production of diphenylurea and dibenzylurea, respectively. An expanded substrate scope including the electron-rich and electron-deficient anilines, primary aliphatic amines, secondary amines was also established. This work offers a straightforward, step economic, and green methodology for the efficient synthesis of valuable ureas.
View More


Sichuan Sangao Biochemical Co., Ltd
Contact:+86-28-84874233
Address:19F, Bldg.2, Shudu Center, Tianfu 2nd St., Hi-tech zone, Chengdu 610041, Sichuan Province, China.
Qingdao XinYongAn Chemicals Co., Ltd
Contact:+86-532-81107967
Address:Chengyang dual-port industrial park by the sea,Qingdao
Yingkou Sanzheng Organic Chemical Co. Ltd.
Contact:+86-417-3638818
Address:25 Gengxinli Village, Daqing Road, Yingkou, Liaoning, China
Oren Hydrocarbons (Qingdao) Co., Ltd.
Contact:+86-532-68607667-801
Address:Room 3 # 302, No.9 Qingyun Road, Qingdao, China
Shanghai Pinewood Fine Chemical Co., Ltd.
website:http://www.pinewoodchem.com
Contact:0086-21-62417129,62414096
Address:Suite B, 27F, No.2, Lane 600, Tianshan Road, Shanghai
Doi:10.1016/j.jcat.2005.07.022
(2005)Doi:10.1021/jo00344a006
(1982)Doi:10.1002/(SICI)1096-9888(199711)32:11<1236::AID-JMS584>3.0.CO;2-K
(1997)Doi:10.1016/S0040-4039(01)95055-5
(1978)Doi:10.1039/c9cy01259a
(2019)Doi:10.1007/BF00909864
(1974)